Фенол и анилин - два химических соединения, которые на первый взгляд могут показаться похожими. Однако, они обладают различными свойствами и проявляют разные химические реакции. Одно из ключевых отличий между ними заключается в их реакции с водой и рН-значениях. Фенол обладает кислотными свойствами, а анилин - основными.
Фенол является ароматическим алкоголем, состоящим из группы гидроксильных и ароматических. Именно группа гидроксильных, состоящих из атома кислорода и атома водорода, делает его кислотным. Когда фенол растворяется в воде, он образует ион гидроксида и ионы водорода, что позволяет ему проявлять кислотные свойства. Помимо этого, фенол образует стабильные соединения с щелочами, обеспечивая свое кислотное поведение.
Кислотность фенола также проявляется в его растворимости в воде. Фенол растворим в воде в отличие от других гидроксидов алкилов и арилов, так как группа гидроксильных остатков обладает положительными зарядами на атоме кислорода, образуя водородные связи с молекулами воды. Это позволяет фенолу образовывать гидраты, укрепляя его растворимость.
Анилин относится к классу аминоароматических соединений. Это амин, состоящий из одной группы амино. Группа амино характеризуется присутствием атома азота, который обладает свободной парой электронов. Эта пара электронов делает анилин основным соединением. Оно способно принимать протоны от кислых соединений, что свидетельствует о его щелочных свойствах.
Фенол и анилин: почему они имеют кислотные и основные свойства?

Фенол содержит в своей структуре гидроксильную группу (-OH), которая обуславливает его кислотные свойства. Гидроксильная группа способна отдавать протон, что приводит к образованию отрицательно заряженного иона. У фенола имеется еще одна важная особенность – наличие ароматического кольца, которое также усиливает его кислотные свойства.
Анилин, в свою очередь, содержит аминогруппу (-NH2), которая является основным фрагментом молекулы. Аминогруппа обладает способностью принимать протон, образуя положительно заряженный ион. Эта особенность делает анилин основным соединением.
Почему гидроксильная группа в феноле обладает кислотными свойствами, а аминогруппа в анилине – основными? Хотя оба соединения содержат протонную функцию, их химические свойства различаются из-за разных электронных структур.
В феноле гидроксильная группа находится вблизи ароматического кольца, что делает молекулу фенола более структурно стабильной. В результате такого расположения, возникает возможность слабой депротонирования – отдачи протона. Это обуславливает кислотные свойства фенола.
В анилине аминогруппа не находится возле ароматического кольца и между ними присутствует электронный перенос. Это делает молекулу анилина менее структурно стабильной и уменьшает возможность аминогруппы принимать протон. Именно поэтому анилин обладает основными свойствами.
- Фенол является слабой кислотой за счет стабильности молекулы и возможности отдать протон.
- Анилин является слабой основой из-за нестабильности его молекулы и ограниченной способности принять протон.
Таким образом, химические свойства фенола и анилина определяются разной расположенностью функциональных групп и электронной структурой молекулы. Это позволяет фенолу обладать кислотными свойствами, а анилину – основными.
Фенол - кислотное соединение, а анилин - основное вещество
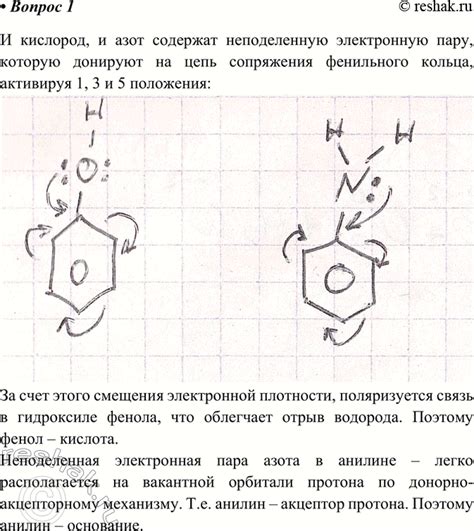
Анилин, в отличие от фенола, является основным веществом. Это обусловлено наличием аминогруппы (-NH2) в его молекуле. Амино-группа обладает свойством принимать протон, что позволяет анилину образовывать ионы анилиния (C6H5NH3+) в водных растворах.
Таким образом, различие в кислотных или основных свойствах фенола и анилина обусловлено разными функциональными группами в их молекулах: гидроксильной группой (-OH) в феноле и аминогруппой (-NH2) в анилине.
Почему фенол обладает кислотными свойствами?

Кислотность фенола объясняется наличием нескольких факторов:
- Карбоксильная группа (-OH) обладает способностью отдавать протоны (H+). В молекуле фенола присутствует эта группа, и поэтому фенол может выступать в реакциях как кислота.
- Гидроксильная группа делает фенол более поларным соединением, что усиливает его кислотные свойства. Полярная группа притягивает основания, способствуя передаче протона.
- Бензольное кольцо в феноле обладает минусовым зарядом, что делает молекулу стабильной и способной отдавать протоны.
Из-за указанных свойств фенол может реагировать с основаниями, образуя соли. Например, в реакции с натрием фенол образует натриевую соль – фенолат натрия (C6H5ONa).
Кислотные свойства фенола являются одной из причин его широкого применения в промышленности и научных исследованиях.
Какие группы атомов в феноле отвечают за его кислотность?

Гидроксильная группа (-OH) в феноле придаёт ему кислотные свойства, так как способна образовывать водородные связи с молекулами воды или другими соединениями. Когда фенол вступает в реакцию с щелочами (например, гидроксидом натрия NaOH), гидроксильная группа отдаёт протон (H+) и образуется ион фенолата, который имеет отрицательный заряд. Именно эта реакция доказывает кислотность фенола.
Ароматическая группа в феноле не отвечает за его кислотность, так как взаимодействие с щелочами происходит именно через гидроксильную группу. Кислотность фенола отличает его от других ароматических соединений, таких как бензол, которые не обладают кислотными свойствами.
Фенол - слабая кислота: причины и механизмы
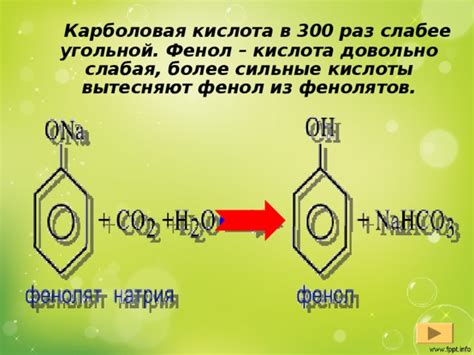
Причиной слабой кислотности фенола является наличие ароматического цикла, состоящего из шести атомов углерода. У ароматических соединений электроны "делокализованы", то есть они свободно перемещаются по всей молекуле. В результате, электроны не являются сильно связанными с отдельными атомами углерода, и снижается положительный заряд на атоме кислорода, а следовательно, и его избыточный негативный заряд. Это снижает способность фенола отдавать протоны, делая его слабой кислотой.
Основным фактором, делающим фенол слабой кислотой, является отталкивание заместителей, находящихся в позиции орто или пара (направление, в котором находятся атомы или группы атомов относительно основной части молекулы). В присутствии этих заместителей, гидроксильная группа в феноле становится слабее кислотной. Это происходит из-за влияния заместителей, которые могут оказывать электронные и пространственные эффекты, что затрудняет отдавание протона.
Таким образом, слабая кислотность фенола обусловлена его молекулярной структурой и влиянием ароматического цикла и замещающих групп на способность отдавать протоны. Это отличает фенол от других более кислотных соединений, таких как анилин, который является слабой основой.
Анилин - слабая основа: причины и механизмы
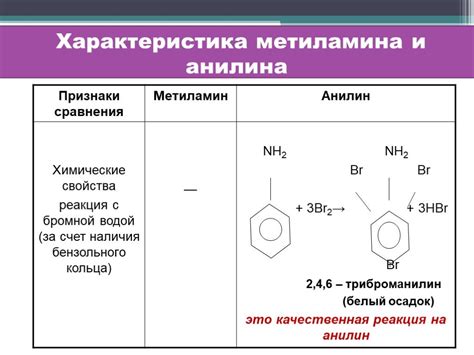
Одной из причин, почему анилин является слабой основой, является наличие электроотрицательного атома кислорода в аминогруппе, который обладает сильными электроотрицательными свойствами. Это приводит к деликатному равновесию между двумя основными формами молекулы - нейтральной и лишенной протона (депротонированной) аминогруппы.
Также, анилин обладает высокой конъюгацией в ароматическом кольце, что влияет на объединение пи-электронов и уменьшает доступность аминогруппы для протонирования. Поэтому, анилин стремится сохранить полностью конъюгированную систему электронных облаков, что ослабляет его основные свойства.
Механизм протонирования анилина также объясняет его слабость как основы. Протонирование происходит за счет передачи протона от кислоты к анилину. Однако, в данном случае, молекула анилина образует затрудненную 4-членную фрагментацию при протонировании, что является энергетически невыгодным процессом.
Таким образом, структурные и электронные характеристики анилина объясняют его слабые основные свойства. Они ограничивают возможность анилина взаимодействовать с кислотами и придает ему менее выраженный основной характер по сравнению с фенолом.
Какие группы атомов в анилине отвечают за его основность?

Аминогруппа, состоящая из атома азота и двух атомов водорода, является донором электронов. Благодаря наличию свободной пары электронов у атома азота, анилин может образовывать аммонийные ионы, что позволяет ему проявлять основные свойства.
Ароматическое кольцо, составленное из шести углеродных атомов, также влияет на основность анилина. Ароматическое кольцо обладает необычными электронными свойствами, что делает анилин основным.
Реакции фенола и анилина, связанные с их кислотными и основными свойствами
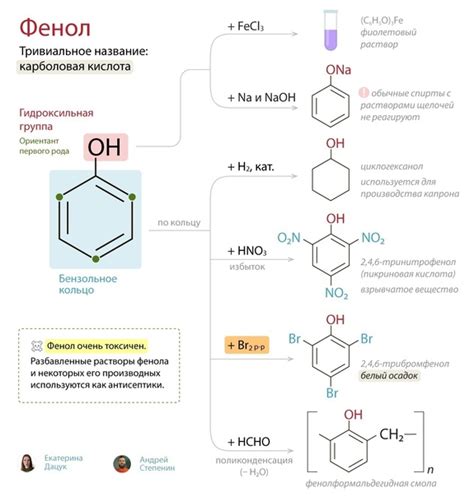
Фенол обладает кислотными свойствами из-за наличия гидроксильной группы. Гидроксильная группа вступает в реакцию с натрием, алюминием, желез(III) хлоридом и другими агентами, что позволяет производить производные фенола, включая различные фенолаты и эфиры. Эта кислотность проявляется в способности фенола образовывать стабильные соли с щелочными металлами, например, натрием. Соединение также реагирует с окислителями, к примеру, с перманганатом калия.
С другой стороны, анилин обладает основными свойствами из-за наличия аминогруппы. Аминогруппа вступает в реакцию с кислотами, например, с соляной кислотой и серной кислотой, образуя соли, такие как анилиниум-хлорид. Основность анилина также проявляется в способности соединения образовывать стабильные соли с кислотными окислителями, например, с перманганатом калия или хлорующей серной кислотой.
Обе молекулы обладают состояниями резонанса, которые объясняют их способности проявлять кислотные или основные свойства. В случае фенола, резонансное удержание электрона на атому кислорода делает его более электроотрицательным и способствует образованию отрицательного заряда. В случае анилина, резонансное удержание электрона на атому азота отнимает электроны от ароматического кольца, что приводит к формированию положительного заряда.
Реакции фенола и анилина, связанные с их кислотными и основными свойствами, представляют собой важные аспекты в органической химии. Эти реакции могут быть использованы для синтеза новых соединений и молекул, а также для исследования и понимания химических свойств и поведения фенола и анилина.
Значение фенола и анилина в органическом синтезе и промышленности

Фенол (гидроксибензол) обладает кислотными свойствами из-за наличия гидроксильной группы (-OH). Он является слабой кислотой, поскольку способен отдавать протон (Н+) в реакциях с основаниями. Фенол активно используется в органическом синтезе, включая процессы получения пластмасс, резин, лекарственных препаратов и других важных химических веществ. Также фенол используется в производстве фенол-формальдегидных смол, которые широко применяются в промышленности.
Анилин (фениламин) является основанием за счет амино-группы (-NH2), которая способна принимать протон (Н+) в реакциях с кислотами. Анилин широко используется в органическом синтезе для получения различных соединений, включая красители, лекарственные вещества, пластмассы и другие важные соединения. Он также используется в производстве резины, пестицидов и других продуктов промышленности.
Оба соединения имеют широкий спектр применения в различных областях, и их значение в органическом синтезе и промышленности трудно переоценить. Их уникальные свойства и разнообразные реакционные возможности делают фенол и анилин ценными компонентами в синтезе различных органических соединений и материалов.